ENADE 2021 - QUESTÃO 23 A Teoria dos Orbitais Moleculares (TOM) para moléculas poliatômicas, aplicando a Teoria de Grupos nas combinações li...
ENADE 2021 - QUESTÃO 23
A Teoria dos Orbitais Moleculares (TOM) para moléculas poliatômicas, aplicando a Teoria de Grupos nas combinações lineares dos orbitais atômicos, aborda a química estrutural considerando os elétrons espalhados sobre toda a molécula.
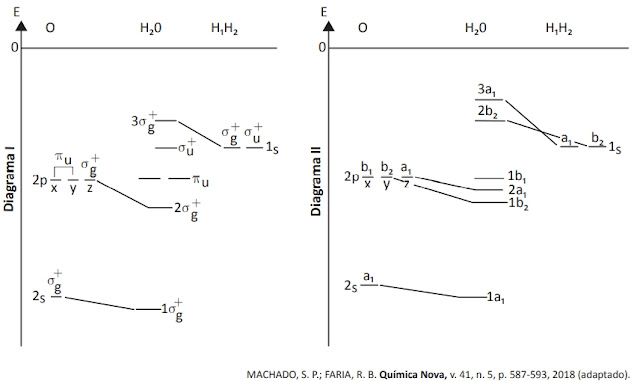
Os níveis de energia dos orbitais moleculares podem ser previstos com as correlações de Walsh ou com a abordagem alternativa, que aplica os princípios de simetria da teoria de grupo para a construção dos diagramas qualitativos, como exemplificados a seguir (sem os elétrons) para a molécula da H2O.
Após preencher os diagramas apresentados com os elétrons, avalie as afirmações a seguir.
I. Os orbitais πu não possuem contribuição dos orbitais 1s do hidrogênio.
II. O diagrama II representa os níveis de energia dos orbitais moleculares da H2O com geometria D∞h.
III. O HOMO (orbital molecular ocupado de mais alta energia) da H2O no diagrama II corresponde ao b1.
IV. O LUMO (orbital molecular desocupado de mais baixa energia) da H2O no diagrama I corresponde ao .
.
É correto apenas o que se afirma em
A) I e II.
B) II e IV.
C) III e IV.
D) I, II e III.
E) I, III e IV.
QUESTÃO ANTERIOR:
GABARITO:
E) I, III e IV.
RESOLUÇÃO:
Não temos resolução para essa questão! Você sabe explicar? Copie o link dessa página e envie sua resolução clicando AQUI!
PRÓXIMA QUESTÃO:
QUESTÃO DISPONÍVEL EM: